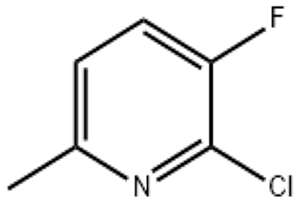
2-cloro-3-fluoro-6-picolina (CAS# 374633-32-6)
Introducción
Apariencia: Generalmente líquido de incoloro a amarillo claro, estas características de apariencia implican que puede ser sensible a la luz y al calor, y es necesario tomar medidas para evitar el control de la luz y la temperatura durante el almacenamiento y transporte, como usar botellas de vidrio marrón y almacenarlas. en un almacén fresco para evitar que el color se intensifique y se deteriore aún más.
Solubilidad: El compuesto tiene buena solubilidad en disolventes orgánicos comunes, como tolueno y diclorometano, sigue el principio de solubilidad similar y tiene afinidad con disolventes orgánicos en virtud de la parte hidrófoba de la molécula; Sin embargo, la solubilidad en agua es baja y es difícil que la molécula rompa eficazmente los fuertes enlaces de hidrógeno entre las moléculas de agua, lo que dificulta su dispersión.
Punto de ebullición y densidad: los datos del punto de ebullición están estrechamente relacionados con su volatilidad y pueden proporcionar parámetros clave para operaciones como la destilación y la purificación, pero desafortunadamente el valor específico del punto de ebullición no se ha divulgado ampliamente. Su densidad es ligeramente mayor que la del agua, y comprender la densidad puede ayudar a estimar con precisión la relación de conversión de volumen-masa en operaciones experimentales o procesos industriales como la transferencia de líquidos y la medición precisa.
Propiedades químicas
Reacción de sustitución: el átomo de cloro y el átomo de flúor en la molécula son los sitios reactivos potenciales. En la reacción de sustitución nucleófila, los nucleófilos fuertes pueden atacar los sitios donde se encuentran los átomos de cloro y flúor, reemplazar los átomos correspondientes y generar nuevos derivados de piridina. Por ejemplo, se ha combinado con algunos nucleófilos que contienen nitrógeno y azufre para desarrollar una serie de compuestos heterocíclicos que contienen nitrógeno con estructuras más complejas para el descubrimiento de fármacos o la síntesis de materiales.
Reacción redox: el anillo de piridina en sí es relativamente estable, pero cuando se combinan oxidantes fuertes, como el permanganato de potasio y el peróxido de hidrógeno, con condiciones ácidas, puede ocurrir oxidación, lo que resulta en la destrucción o modificación de la estructura del anillo de piridina; Por el contrario, con un agente reductor adecuado, como por ejemplo hidruros metálicos, es teóricamente posible la hidrogenación de enlaces insaturados intramoleculares.
Cuarto, el método de síntesis.
La ruta de síntesis común es comenzar a partir de derivados de piridina simples y construir gradualmente la estructura objetivo mediante reacciones de halogenación y fluoración. En primer lugar se metilan selectivamente los compuestos de piridina, que son el material de partida, y al mismo tiempo se introducen los grupos metilo; Luego utilizar reactivos de halogenación, como cloro y cloro líquido, con catalizadores y condiciones de reacción adecuados, para lograr la introducción de átomos de cloro; Finalmente, se utilizaron reactivos fluorados, como Selectfluor, para fluorar con precisión el sitio objetivo y obtener 2-cloro-3-fluoro-6-metilpiridina.
Usos
Intermedios de síntesis de fármacos: los químicos medicinales adoran su estructura única y es un intermediario de alta calidad para el desarrollo de nuevos fármacos antibacterianos, antivirales y antitumorales. Las propiedades electrónicas y la estructura espacial de los anillos de piridina y sus sustituyentes pueden unirse específicamente a proteínas diana in vivo y se espera que se transformen en ingredientes activos con excelente eficacia después de una modificación posterior en varios pasos.
Ciencia de los materiales: en el campo de la síntesis de materiales orgánicos, se puede utilizar para fabricar materiales poliméricos funcionales, materiales fluorescentes, etc., en virtud de su capacidad para introducir con precisión cloro, átomos de flúor y estructuras de piridina, dotar a los materiales de propiedades eléctricas y ópticas especiales. propiedades y promover el desarrollo de tecnologías de vanguardia, como materiales inteligentes y materiales de visualización.